Nutrição de precisão
O Projeto Genoma Humano desencadeou avanços importantes na área da saúde, e a nutrição foi fortemente influenciada através da consolidação da genômica nutricional. O conhecimento da genética relacionada à nutrição faz parte dos grandes estudos na nutrição de precisão ou nutrição individualizada para prevenção de doenças.
Nos últimos tempos ocorreram importantes mudanças no objetivo das pesquisas nutricionais, que antes eram focadas nas doenças carênciais, para aquelas com manifestações clínicas metabólicas, como por exemplo obesidade, diabetes e doença cardiovascular têm sido beneficiadas pelos estudos moleculares.
Uma das faces da genômica nutricional é a nutrigenética, que estuda a influência da variabilidade genética entre os indivíduos sobre as necessidades nutricionais, estado de saúde e risco de desenvolver doenças. O foco da nutrigenética é entender os efeitos das variações que existem no DNA, incluindo os polimorfismos de nucleotídeo único (SNPs), variações de número de cópias (CNV) e polimorfismos de inserção ou deleção (INDEL) nas respostas biológicas à ingestão alimentar e a influência no estado e risco de doença.
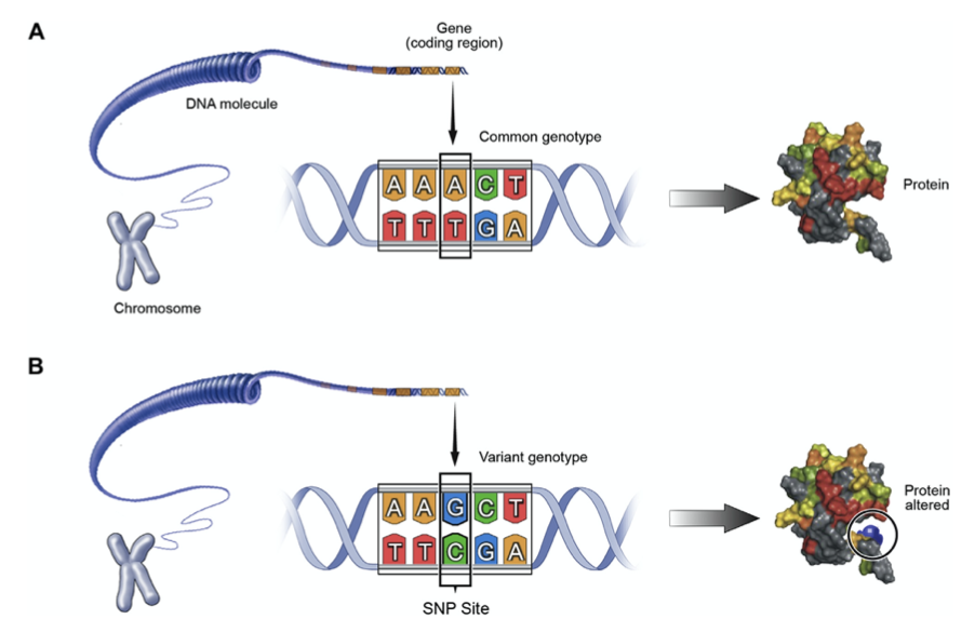
Alguns SNPs são nutricionalmente relevantes, como o que envolve o status de folato e homocisteína. O polimorfismo C677T é um SPN comum do gene metiltetrahidrofolato redutase (MTHFR), que codifica a enzima 5,10-MTHFR e usa o folato para metabolizar e reciclar a homocisteína. Os indivíduos portadores do genótipo TT neste gene tem a redução da eficiência enzimática levando a reduzidos níveis de folato, e elevação em cerca de 20% os níveis de homocisteína no sangue, quando os comparados com os portadores do genótipo CC, mais comum. Este polimorfismo está associado a um aumento de risco de doença cardiovascular, assim como a deficiências no fechamento do tubo neural em fetos de gestantes portadoras do mesmo. Além disso, folato, metionina e colina estão envolvidos na metilação do DNA, RNA e proteínas, quando há desequilíbrio em um destes, resulta em modificações compensatórias nos demais.
Outra questão de interesse primordial para a nutrição é a propensão genética para o desenvolvimento de obesidade e sobrepeso, inflamação, dislipidemia e estresse oxidativo, todos também influenciados pela exposição ambiental, como a dieta e estilo de vida. A obesidade grave pode ser causada por mutações em apenas um gene, mas na maioria dos casos populacionais ela é poligênica, envolvendo complexas interações entre genes e ambiente.
Variantes no gene FTO têm sido associados à obesidade em estudos de associação genômica ampla. Este gene codifica uma proteína com ação de enzima demetilase de RNA e DNA. Muito importante na epigenética do RNA. Estudos indicam um envolvimento na via do hormônio grelina. O FTO é expresso em diferentes tecidos humanos, com maiores quantidades de mRNA expressos no núcleo arqueado do hipotálamo. Além de potencializar fatores de transcrição envolvidos na adipogênese e associar-se com a sensibilidade a insulina no córtex cerebral, esse gene está fortemente associado a obesidade, relacionando-se com diferenças no comportamento alimentar, saciedade e ingestão de alimentos. Expressão regulada pelo ciclo jejum/alimentação sendo que aqueles que possuem o genótipo AA tem tendência a maior peso corporal do que aqueles que não possuem o alelo de risco. Este risco pode ser modificado pela atividade física e pela redução de ingestão de energia.
Outro gene fundamental para os estudos metabólicos é o MC4R, que expressa um receptor acoplado proteína G transmembrana (332 aminoácidos). As mutações neste gene são responsáveis por 6-8% da obesidade monogênica. É expresso no centro da fome do cérebro. Apresenta papel crítico no eixo leptina/melanocortina que regula também a ingestão alimentar. É um regulador da homeostase energética: hiperfagia e ingestão de alimentos com alto teor calórico. Tem função no controle da saciedade. A interrupção da sinalizacão da melanocortina no hipotálamo reduz a sensação de saciedade e pode levar a uma redução da atividade física e aumento da obesidade.
O gene PPARG codifica receptores transmembrana. O PPAR-gama é expresso no tecido adiposo, baço, adrenais e cólon e células do sistema imune. Ácidos graxos Poliinsaturados são ligantes naturais de PPARs. Metabólitos de ácidos graxos (oxidados ou eicosanóides) também são ligantes. Após a ligação do ativador, ocorre a mudança conformacional do receptor, resultando na formação do heterodímero com o receptor de retinóide X (RXR) na região promotora do gene alvo, permitindo o recrutamento de co-ativadores e o desligamento de co-repressores, resultando na transcrição gênica. Mas os PPARs podem também reprimir a expressão gênica por interferirem em outros fatores de transcrição, como NF-kB, proteína ativadora (AP-1) e a proteína estimuladora de ligação de CCAAT.
A Biogenetika realiza análise genética destes marcadores abordados, assim como diversos outros relacionados à nutrição, que se mostram essenciais para um atendimento com foco na nutrição individualizada. Conte com a nossa tecnologia e conhecimento técnico para atender de forma completa seu paciente!
REFERÊNCIAS:
COMINETTI, Cristiane; HORST, Maria Aderuza; ROGERO, Marcelo Macedo. Brazilian Society for Food and Nutrition position statement: nutrigenetic tests. Nutrire, [S.L.], v. 42, n. 1, p. 1-11, 5 abr. 2017. Springer Science and Business Media LLC. http://dx.doi.org/10.1186/s41110-017-0033-2.
CAMP, Kathryn M.; TRUJILLO, Elaine. Position of the Academy of Nutrition and Dietetics: nutritional genomics. Journal Of The Academy Of Nutrition And Dietetics, [S.L.], v. 114, n. 2, p. 299-312, fev. 2014. Elsevier BV. http://dx.doi.org/10.1016/j.jand.2013.12.001.