
APOE ε4: além do Alzheimer
Doenças neurodegenerativas, como Alzheimer (DA), Parkinson (DP), Esclerose lateral amiotrófica (ELA), demência frontotemporal (DFT) e outras condições afetam mais de 57 milhões de pessoas em todo o mundo, e as previsões são de que dobrem a cada 20 anos. Já é possível fornecer aos pacientes tratamentos direcionados que, combinados, podem prevenir, retardar, interromper ou reverter a progressão da doença. Entretanto, obstáculos importantes atrasam o início do tratamento. As doenças neurodegenerativas têm um período pré-clínico ou prodrômico prolongado, onde o diagnóstico, usando avaliações baseadas em sintomas disponíveis não é possível ou extremamente difícil devido a manifestações sutis que não são detectáveis pelas ferramentas clínicas atuais.
Há também a heterogeneidade na concordância entre a patologia molecular e a síndrome clínica, bem como a ocorrência frequente de múltiplas patologias que contribuem para diagnósticos equivocados em ambientes clínicos. Ainda, há a variabilidade adicional na taxa e no padrão de progressão dos sintomas dentro das condições, impedindo os esforços para indicar o prognóstico do curso da doença com precisão. Estes desafios diagnósticos e prognósticos dificultam o tratamento bem-sucedido de pacientes em estágios precoces da doença.
Abordagens multiômicas, integrando a genômica, trancriptômica, proteômica e metabolômica contribuem de forma única para impactar o diagnóstico e o tratamento de doenças neurodegenerativas. Em um esforço global, o Global Neurodegenerative Project Consortium (GNPC), reuniu uma coorte mundial de mais de 35 mil bioamostras analisadas e publicou um estudo, em abril de 2025, com os dados da versão 1 desta análise, que se concentra em entender a relação entre o envelhecimento e as doenças neurodegenerativas DA, DP, ELA e DFT.
Como um dos resultados deste grande esforço internacional, a análise do genótipo APOE em todo proteoma revelou uma assinatura da APOE alelo ε4 robusta e independente da doença, com potencial relevância mecanicista para a proteostase e o transporte de lipídeos. A variante ε4 (alelo ε4) do gene da apolipoproteína E (APOE ε4) está bem estabelecida como o maior fator de risco genético para a DA de início tardio. No entanto, evidências crescentes indicam que o transporte de APOE ε4 também pode ter um papel em outras doenças neurodegenerativas associadas à idade. Estudos associaram APOE ε4 ao aumento do risco e à menor idade de início da DFT, DP e ELA. O alelo ε4 está associado a uma taxa mais rápida de declínio cognitivo e cognição deficiente da DP, aumentando o risco de demência da DP.
Utilizando o líquido cefalorraquidiano (LCR) e o plasma, foram realizadas análises proteômicas em indivíduos com DA, DP, DFT, ELA e em controles não comprometidos, assim como análises do córtex pré-frontal e marcadores post-mortem (placas beta-amiloides, emaranhados neurofibrilares de tau, gliose e angiopatia, TDP-43 e alfa-sinucleína) de doadores com as doenças. Foram analisadas variáveis clínicas e de estilo de vida, como hipertensão, tabagismo e diabetes, para possíveis interações entre proteínas e APOE ε4, como pode ser visto no desenho do estudo na Figura 1.
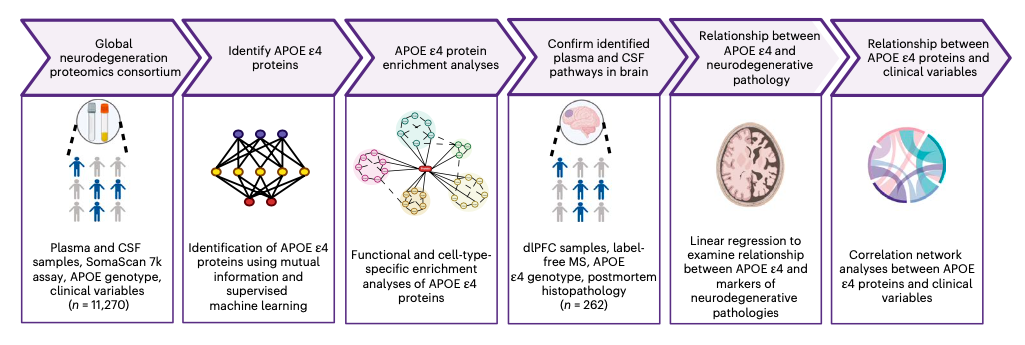
Figura 1. Desenho do estudo para identificar e caracterizar alterações sistêmicas do proteoma em portadores de APOE ε4.
Os resultados demonstraram que que todos os portadores de APOE ε4, independentemente da doença neurodegenerativa, têm uma assinatura proteômica conservada e única que se estende pelo plasma, LCR e cérebro. Essa assinatura está associada à desregulação imunológica pró-inflamatória e ao enriquecimento de células imunes circulantes, incluindo monócitos, células T CD8 e γδ de memória, Tregs e células NK. Esse fenótipo molecular se estende aos cérebros de portadores de APOE ε4 de maneira semelhante, independente da doença, e não está associado à presença de nenhuma patologia cerebral específica da doença, como pode ser visto no esquema da Figura 2. Portanto, o fenótipo molecular pró-inflamatório associado a APOE ε4 foram espelhados no SNC, e se estende a indivíduos com outras doenças neurodegenerativas, incluindo DFT, DDP, DP e ELA. Neste estudo, o status de APOE ε4 não foi associado às características marcantes das patologias, incluindo β-amiloide, tau, TDP-43 ou α-sinucleína, nos respectivos grupos de doenças.
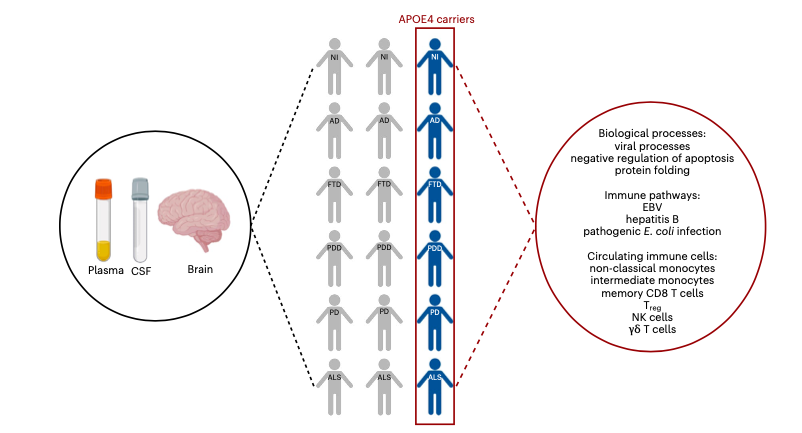
Figura 2. APOE ε4 carriers across different neurodegenerative diseases share a common systemic proteomic change reflective of pro-inflammatory immune dysregulation.
Ainda descobriram que, embora todos os portadores de APOE ε4 tenham uma assinatura proteômica sistêmica relacionada ao sistema imunológico, as relações entre as proteínas dentro dessa assinatura estão exclusivamente associadas a variáveis demográficas, de estilo de vida e clínicas de maneira específica para doenças neurodegenerativas. Isso sugere que, embora as alterações biológicas associadas ao portador de APOE ε4 sejam essenciais para a neurodegeneração, de modo geral, as interações com a vulnerabilidade biológica subjacente e o ambiente podem ser fundamentais para impulsionar a patogênese da doença neurodegenerativa específica.
De forma interessante, os autores do artigo trazem evidências de que o genótipo APOE ε4 seja um exemplo moderno de pleiotropia antagônica. Portanto, em adultos mais jovens, a APOE ε4 está associada ao aumento de sobrevida e da fertilidade em ambientes com altos níveis de doença infecciosa. Dessa forma, os indivíduos saudáveis heterozigotos para APOE ε4 apresentam liberação aumentada de citocinas, níveis plasmáticos de TNF aumentados, uma resposta hipertérmica mais pronunciada e um início mais precoce da produção de IL-6 após desafio imunológico com ligantes TLR2/TLR4/TLR5 ou lipopolissacarídeo (LPS), com maior proteção em casos de infecções. Entretanto, embora essa resposta imune proteja os portadores mais jovens de APOE ε4 de doenças infecciosas, estados prolongados de inflamação e liberação de citocinas são provavelmente deletérios com a idade.
Estes resultados corroboram com a reconceitualização de APOE ε4 como um alelo de suscetibilidade mais amplo, contribuindo para mecanismos patogênicos compartilhados entre doenças neurodegenerativas. No entanto, ainda não está claro por que APOE ε4 está mais fortemente associado à DA em termos de prevalência, apesar de exibir efeitos biológicos sistêmicos em doenças neurodegenerativas. Assim, embora APOE ε4 confira uma suscetibilidade biológica compartilhada, a expressão da doença provavelmente depende de uma combinação de antecedentes genéticos, contexto(s) celular(es) e exposições ao longo da vida.
Embora os mecanismos exatos subjacentes ao espelhamento dos estados pró-inflamatórios periféricos e centrais permaneçam obscuros, eles podem envolver interações entre células imunes periféricas pró-inflamatórias e à barreira hematoencefálica (BHE). Em apoio a isso, portadores de APOE ε4 cognitivamente saudáveis exibem um fenótipo pró-inflamatório sistêmico, marcadores precoces de disfunção da BHE no hipocampo e no lobo temporal medial., alterações na atividade e conectividade cerebral e distúrbios do sono. À medida que a BHE se torna cada vez mais comprometida, ela permite a infiltração de proteínas derivadas do sangue e células imunes pró-inflamatórias no cérebro, contribuindo para a neuroinflamação e neurodegeneração exacerbadas. Os pesquisadores identificaram subpopulações enriquecidas de células imunes pró-inflamatórias, incluindo monócitos não clássicos e intermediários, células T CD8+ de memória, células T γδ e células NK. Esses tipos de células imunes podem representar células mononucleares do sangue periférico que interagem com a BHE para promover a neurodegeneração em portadores de APOE ε4.
Se todos os portadores de APOE ε4 compartilham uma vulnerabilidade biológica subjacente comum à neurodegeneração, uma questão importante é o que determina qual doença neurodegenerativa específica eles desenvolvem. Isso provavelmente reflete interações complexas entre risco genético e exposições ambientais, incluindo hipercolesterolemia e doença cardíaca isquêmica, independente de comorbidades cardiovasculares. Os resultados sugerem que insultos ambientais ou patológicos adicionais podem atuar sinergicamente com um estado pró-inflamatório geneticamente preparado para impulsionar a neurodegeneração em portadores de APOE ε4. Ainda, indivíduos com doenças neurodegenerativas também podem ter maior probabilidade de desenvolver comorbidades, como hipertensão, que pode ser consequência do processo neurodegenerativo e não um evento precursor.
Desta forma, o grupo de autores, defende a ideia de que é preciso alterar a compreensão conceitual, relacionada ao gene APOE e outras variantes genéticas de risco, como específica para a DA, passando a reconhecer seus potenciais como modificadores pleiotrópicos compartilhados da vulnerabilidade neurodegenerativa. Portanto, APOE ε4 é entendido como um modulador imunológico pleiotrópico.
O teste genético BioAlzheimer da Biogenetika identifica com precisão a presença do alelo APOE ε4, o principal fator de risco genético para Alzheimer e outras doenças neurodegenerativas. Detectar essa vulnerabilidade de forma antecipada permite adotar estratégias personalizadas de prevenção, acompanhamento e intervenção antes do surgimento dos sintomas, potencialmente retardando ou evitando a progressão da doença. Com base em evidências científicas recentes e análise de marcadores moleculares, o BioAlzheimer oferece informação valiosa para proteger sua saúde cognitiva e qualidade de vida ao longo dos anos.
REFERÊNCIAS:
IMAM, Farhad; SALONER, Rowan; VOGEL, Jacob W.; KRISH, Varsha; ABDEL-AZIM, Gamal; ALI, Muhammad; AN, Lijun; ANASTASI, Federica; BENNETT, David; BINETTE, Alexa Pichet. The Global Neurodegeneration Proteomics Consortium: biomarker and drug target discovery for common neurodegenerative diseases and aging. Nature Medicine, [S.L.], p. 1-23, 15 jul. 2025. Springer Science and Business Media LLC. http://dx.doi.org/10.1038/s41591-025-03834-0.
SHVETCOV, Artur; JOHNSON, Erik C. B.; WINCHESTER, Laura M.; WALKER, Keenan A.; WILKINS, Heather M.; THOMPSON, Terri G.; ROTHSTEIN, Jeffrey D.; KRISH, Varsha; IMAM, Farhad B.. APOE ε4 carriers share immune-related proteomic changes across neurodegenerative diseases. Nature Medicine, [S.L.], p. 1-24, 15 jul. 2025. Springer Science and Business Media LLC. http://dx.doi.org/10.1038/s41591-025-03835-z.



